Spis treści
- Geny BRCA1 i BRCA2
- Kiedy należy wykonać badanie genetyczne w kierunku określenie nosicielstwa zmian w genach BRCA1 i BRCA2?
- Co w momencie wykrycia zmian w obrębie genów BRCA?
Rak piersi w Polsce stanowi około 22,5% wszystkich zachorowań na nowotwory i jest najczęściej występującymi nowotworem złośliwym u kobiet. W przypadku raka jajnika jest on po raku płuca, piersi i okrężnicy czwartym nowotworem odpowiedzialnym za 4,5% wszystkich przypadków nowotworów, ale jednocześnie powodującym najwięcej zgonów z przyczyn o podłożu nowotworowym. Wpływa na to brak objawów we wczesnym stadium rozwoju oraz brak badań przesiewowych, co często skutkuje diagnozą na zaawansowanym etapie rozwoju i wiąże się z wysoką umieralnością.
Obserwuje się, że około 10% zachorowań na raka piersi i raka jajnika jest związanych z dziedziczeniem uszkodzonych genów, najczęściej są to geny BRCA1 i BRCA2. Analiza nosicielstwa zmian w genach BRCA1 i BRCA2 – mutacji występujących u chorych odgrywa istotną rolę w postępowaniu zapobiegawczym i prognostycznym. Daje informację na temat ryzyka zachorowania na nowotwór, a także pozwala na wdrożenie skutecznych metod profilaktycznych oraz umożliwia wprowadzenie do opieki nad pacjentem bardziej indywidualnego podejścia.
Geny BRCA1 i BRCA2
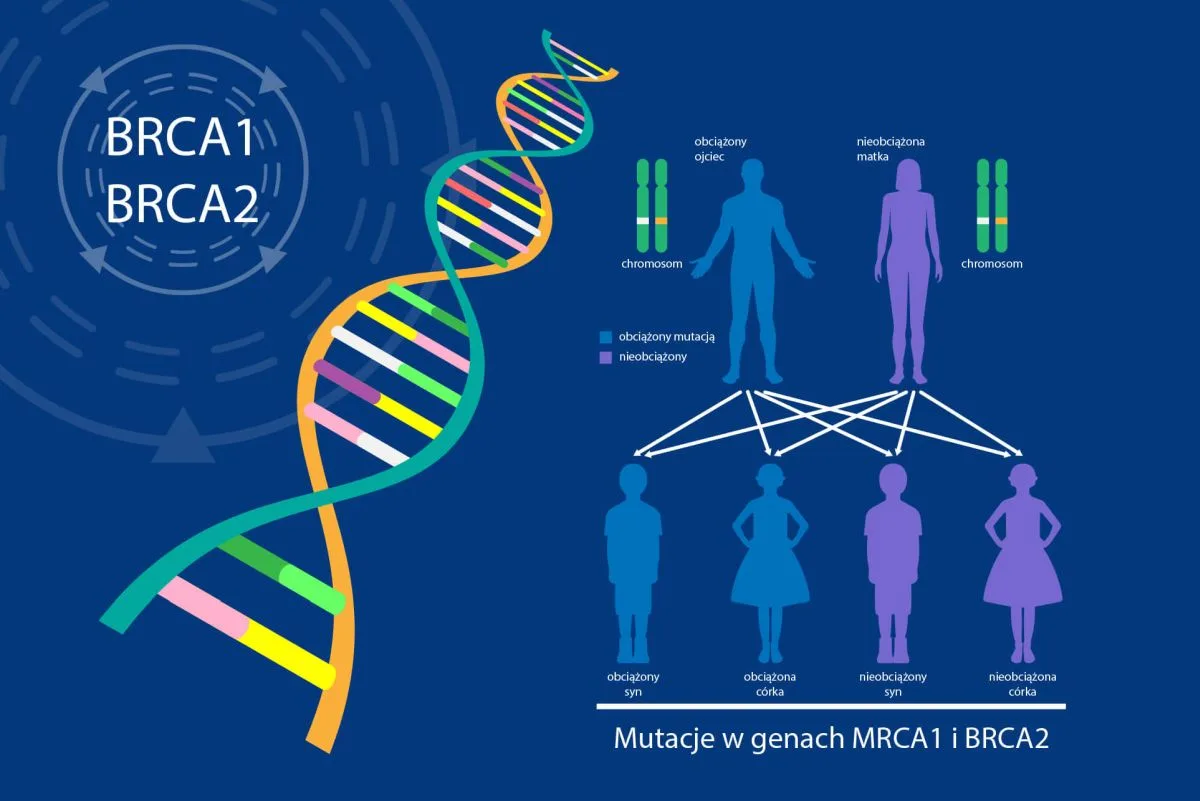
Na podstawie informacji zapisanej w genach BRCA1 i BRCA2 powstają białka, które uczestniczą w procesach naprawy uszkodzeń DNA. Zmiany w obrębie jednego z tych genów sprawiają, że komórki dzielą się w sposób niekontrolowany, w efekcie czego rozwija się nowotwór. U osób, u których występują nieprawidłowe zmiany, obserwuje się również podniesione ryzyko zachorowania na inne nowotwory. Wśród nich możemy wymienić raka trzustki czy raka gruczołu krokowego włączając je do grupy nowotworów BRCA-zależnych. Ryzyko zachorowania na nowotwór zależne jest od rodzaju mutacji, a także jej lokalizacji w genie. Zmiany w obrębie genów BRCA1 czy BRCA2 oprócz zwiększonego ryzyka zachorowania, wiążą się z bardziej agresywną postacią oraz występowaniem nowotworu u pacjentów w młodszym wieku.
Nowotwory BRCA-zależne w 2020 roku przyczyniły się do śmierci ponad 20 tysięcy pacjentów.
Jak wskazują dane, ryzyko zachorowania na raka piersi u nosicielki mutacji w genie BRCA1 określa się na około 50-80%, a w przypadku mutacji w genie BRCA2 to około 40-60%. Dla raka jajnika zmiana w genie BRCA1 to wzrost ryzyka zachorowania na poziomie 20-40%, a dla genu BRCA2 – 40-50%.
Kiedy należy wykonać badanie genetyczne w kierunku określenie nosicielstwa zmian w genach BRCA1 i BRCA2?
Coraz częściej w diagnostyce oraz prewencji wielu chorób wykorzystuje się badania genetyczne, w tym również w profilaktyce nowotworów. Występowanie zmian w obrębie genów jest często jednym z istotniejszych czynników, mogącym wpłynąć na rozwój procesu chorobowego, a ich jak najwcześniejsze wykrycie pozwala na wprowadzenie skutecznych metod, które mogą zapobiec rozwojowi nowotworu.
Takie badanie polega na sprawdzeniu, czy w DNA osoby badanej znajdują się te nieprawidłowości, które powiązane są ze wzrostem ryzyka zachorowania na dany typ nowotworu.
Badanie obecności mutacji w genach BRCA1, BRCA2 zaleca się wykonywać u:
- kobiet z rozpoznanym rakiem piersi,
- kobiet, u których wykryto raka jajnika,
- członków rodzin, jeśli w rodzinie potwierdzona została obecność mutacji w genach BRCA,
- mężczyzn, u których wykryto raka piersi,
- mężczyzn, u których wykryto raka prostaty,
- osób z mnogimi zachorowaniami na raka piersi i/lub jajnika w rodzinie,
- osób, u których wykryto raka trzustki, jeśli posiadają krewną chorą na raka jajnika lub raka piersi, rozpoznanego przed 50. rokiem życia lub dwóch krewnych z rakiem piersi, trzustki lub prostaty.
Takie badanie może ponadto wykonać każda osoba, która chciałaby sprawdzić swoją predyspozycję do zachorowania. Materiałem do badań jest krew żylna, a samo badanie nie wymaga specjalnego przygotowania, osoba badana nie musi być na czczo.


Związek pomiędzy występowaniem mutacji w genach BRCA1 i BRCA2, a zachorowaniem na nowotwory piersi czy jajnika jest znany od dawna. Na przestrzeni lat geny te przebadano pod kątem zmian oraz częstości, z jaką występują w populacji polskiej. Na tej podstawie ustalono najczęściej występujące mutacje zwane także mutacjami założycielskimi. Wszystkie tego typu mutacje mają charakter patogenny, a więc łączą się ze zwiększonym ryzykiem zachorowania na nowotwór. Badanie genetyczne w kierunku wykrycia mutacji założycielskich polega więc na analizie kilku lub kilkunastu miejsc w obrębie genów BRCA1 i/lub BRCA2, które cechują się częstym występowaniem w polskiej populacji.
Należy zwrócić uwagę, że tego typu test jest ściśle ukierunkowany i bada tylko określone zmiany. Zgodnie z Narodowym Programem Zwalczania Chorób Nowotworowych Ministerstwo Zdrowia rekomenduje, aby w przypadku testów BRCA1 zakres badania obejmował 5 mutacji patogennych: c.5266dupC; c.181T>G; c.4035delA; c.66_67delAG; c.3700_3704 del GTAAA. Analizę można rozszerzyć o analizę większej ilości mutacji, które najczęściej występują w polskiej populacji.
Należy pamiętać, że brak mutacji założycielskiej nie wyklucza możliwości istnienia innej mutacji, która występuje w pozostałej części genu, a która nie była analizowana.
W przypadku niewykrycia nosicielstwa mutacji podstawowych (mutacji założycielskich) u osoby chorej na raka piersi i/lub jajnika, która posiada pozytywny wywiad rodzinny można rozszerzyć zakres analizy i wykonać badanie genetyczne w kierunku mutacji BRCA1 oraz mutacji BRCA2 z zastosowaniem sekwencjonowania nowej generacji (NGS). Badanie to daje możliwość zdiagnozowania wszystkich występujących mutacji w analizowanym obszarze genów u danej osoby.

Co w momencie wykrycia zmian w obrębie genów BRCA?
W przypadku stwierdzenia obecności mutacji w genach BRCA osoby znajdują się w grupie tzw. wysokiego ryzyka zachorowania. Wiedza ta umożliwia szybkie wdrożenie takiego schematu postępowania (specjalna opieka lekarska czy odpowiedni program profilaktyczny), by zmniejszyć możliwości rozwoju raka albo też wykryć rozpoczynający się proces nowotworowy jak najwcześniej.
Polskie Towarzystwo Ginekologiczne opracowało dla kobiet, które są nosicielkami mutacji w genach BRCA1 i BRCA2 rekomendacje z zalecaniami profilaktycznymi. Wśród nich znalazło się przede wszystkim częstsze w porównaniu do osób bez mutacji wykonywanie badań kontrolnych, takich jak badanie mammograficzne, badanie ultrasonograficzne piersi, rezonans magnetyczny piersi, badanie ultrasonograficzne przezpochwowe, czy oznaczenie stężenia antygenu nowotworowego 125 (CA125) we krwi.
Korzyści, które płyną z wiedzy o posiadaniu niekorzystnych zmian w genach BRCA, u zdrowych osób mogą przyczynić się do bardziej efektywnego i dostosowanego do danej osoby zarządzania ryzykiem zachorowania. Mamy możliwość pełnego wykorzystania oraz dostosowania dostępnych metod i zabiegów profilaktycznych w sposób optymalny. W przypadku pacjentów, u których nowotwór się już rozwinął, wiedza ta może pomóc w podejmowaniu decyzji terapeutycznych. Znalezienie określonych mutacji daje też niejednokrotnie informację o ryzyku wystąpienia innych nowotworów. Należy pamiętać, że na raka piersi mogą chorować również mężczyźni. Stąd niezwykle istotne jest wykonywanie badań genetycznych u osób, które mają do nich wskazania, a także poszukiwanie mutacji genetycznej wśród krewnych.
Piśmiennictwo:
- Raport „Prewencja i diagnostyka nowotworów BRCA-zależnych”
- Raport” Diagnostyka molekularna w leczeniu nowotworów BRCA-zależnych” MODERN HEALTHCARE INSTITUTE kwiecień 2023r.
- Model prewencji oraz wczesnego wykrywania wybranych, dziedzicznie uwarunkowanych nowotworów w ramach ambulatoryjnej opieki specjalistycznej
- Wojciechowska, U., Didkowska, J., Michałek, I., Olasek, P., Ciuba, A. (2020). Nowotwory złośliwe w Polsce w 2018 roku. Pozyskano z: http://onkologia.org.pl/publikacje/, dostęp z 22.02.2021
- Lubiński, J. (red.) (2018). Genetyka kliniczna nowotworów wskazuje na wzrost ryzyka zachorowania na dany nowotwór.
- Jacek Jassem, Maciej Krzakowski Rak piersi OnkOlOgia w Praktyce klinicznej — edukacja 2018, tom 4, nr 4

