Poniższy artykuł jest zapisem webinaru (cz. 1), który odbył się 15.11.2023 r.
W studio ALAB laboratoria gościliśmy dr Magdalenę Jagiełło, lekarkę endokrynolożkę, która od wielu lat popularyzuje wiedzę na temat układu endokrynnego oraz chorób z tego zakresu na uwielbianym przez wszystkich pacjentów blogu dr Magda, oraz w swoich książkach. Poprosiliśmy panią doktor o odpowiedzi na pytania dotyczące insulinooporności, które zadawali nasi pacjenci.
>>> Przeczytaj też: Zapytaj eksperta – Insulinooporność cz. 2. Diagnostyka insulinooporności
1. Czym naprawdę jest insulinooporność? Czy to jest choroba, czy objaw różnych chorób?
Jest to częsty dylemat pacjentów, którzy czasem słyszą od swojego lekarza pierwszego kontaktu, że „nie ma takiej choroby”, że „jest moda na insulinooporność”. Odpowiadając na pytanie: insulinooporność jest stanem, w którym występują zaburzenia metaboliczne i rzeczywiście może współistnieć z innymi schorzeniami. Generalnie insulinooporność jest związana z cukrzycą, po drugie może być związana z zespołem policystycznych jajników (PCOS). Także insulinooporność rzeczywiście ma związek z innymi chorobami, ale sama w sobie jest rodzajem zaburzenia metabolizmu.
2. Czyli nie jest to choroba? Jeśli mamy insulinooporność, to nie dostaniemy takiego rozpoznania?
Nie, o insulinooporności mówimy jako o stanie, nie jako o jednostce chorobowej. To rzeczywiście bywa powodem nieporozumień, ponieważ pacjent odczuwa dolegliwości, ma objawy, a czasem słyszy od lekarza, że nie ma takiej choroby.

3. Czy jeśli mam rozpoznany zespół policystycznych jajników, to powinnam zrobić badania na insulinooporność?
Generalnie warto, chociaż w definicji zespołu policystycznych jajników nie ma insulinooporności i nie jest to warunkiem wymaganym. Ale bardzo często IO występuje właśnie w tej jednostce chorobowej, także zdecydowanie warto w tym kierunku też pójść. Zwłaszcza jeśli występują objawy, leczenie IO może wspomóc leczenie PCOS. Oczywiście nie każda pacjentka z tą chorobą będzie miała zaburzenia IO, ale wiele tak, dlatego ja zrobiłabym takie badania. Dodam jeszcze, że pacjentka z zespołem policystycznych jajników nie musi być otyła, aby mieć insulinooporność, często są to szczupłe pacjentki.
4. Czy pacjent – dorosły lub dziecko – bez nadwagi lub otyłości może mieć insulinooporność?
Oczywiście najczęściej to są osoby otyłe. Jeśli chodzi o dzieci, to sprawa ma się troszkę inaczej, nie chciałabym wkraczać na pole pediatrii. Generalnie hormony w okresie dojrzewania zachowują się w bardzo różny sposób i czasem jest tak, że stwierdzamy przejściowo wysoką insulinę u dziecka, więc postępowanie jest prowadzone w porozumieniu z pediatrą. U dzieci od 10 lat wzwyż jak najbardziej rozpoznajemy i leczymy insulinooporność, nawet podaje się takim małym pacjentom metforminę. Obecnie jest dużo dzieci z otyłością, więc raczej insulinoporność u dzieci podejrzewamy, gdy mają problemy z wagą, u dzieci z prawidłową wagą raczej insulinoporności nie diagnozujemy.
Mam dużo pacjentek, które pytają o dzieci. Bardzo często jest tak, że to w całej rodzinie jest problem, nie dotyczy on tylko jednej osoby. Wpływają na to kłopoty z odżywianiem i trybem życia, który prowadzi cała rodzina, dochodzą do tego również obciążenia genetyczne.Dlatego jeśli problem dotyczy mamy, warto również zbadać najbliższą rodzinę – siostrę, babcię i właśnie dzieci. Dobrą ilustracją problemu insulinooporności w rodzinie jest krążący w mediach mem, gdzie za otyłymi rodzicami – mamą i tatą – idą trzymające się za ręce, również otyłe dzieci, a za nimi idzie otyły jamnik.

5. Porozmawiajmy o objawach insulinooporności. Powiedziała pani, że kobieta z zespołem policystycznych jajników, jeżeli ma objawy insulinooporności, powinna zrobić badania na isnulinooporność. Jakie to mogą być objawy?
Oczywiście to, co nas najbardziej boli to nadwaga i tłuszcz gromadzący się w okolicy brzucha. Przychodzące do mnie pacjentki chcą schudnąć, nie są zadowolone ze swojej wagi, nie podoba im się, że pojawił się brzuszek i to jest dla nich najważniejsze. Gdy zaczynamy rozmawiać, okazuje się, że występuje senność po posiłkach, pojawia się niepowściągliwa chęć na rzeczy słodkie. Pacjentki dopiero z czasem przyznają się, że budzą się w nocy i zjadają pół opakowania ptasiego mleczka. Ukrywają to nawet przed rodziną. Czasem chęć na słodycze jest tak duża, że pojawia się drżenie rąk i poczucie, że „muszę coś zjeść, bo inaczej zrobi mi się słabo”. Pojawiają się problemy z koncentracją, problemy z pamięcią, drzemki po każdym posiłku. To są objawy, które zawsze można sobie wytłumaczyć, np. przemęczeniem, przepracowaniem, innymi chorobami, menopauzą.
Jak już wspomniałam, pacjenci najczęściej przychodzą, ponieważ chcą schudnąć, rzadko z powodu objawów, a może ich być cała lista. Oczywiście występują również nieprawidłowości w badaniach laboratoryjnych, np. nieprawidłowy lipidogram, często są podwyższone próby wątrobowe. Może pojawić się również stłuszczenie wątroby, które opisuje radiolog w USG – bywa, że od tego zaczyna się poszukiwanie przyczyny podwyższonego poziomu cholesterolu.
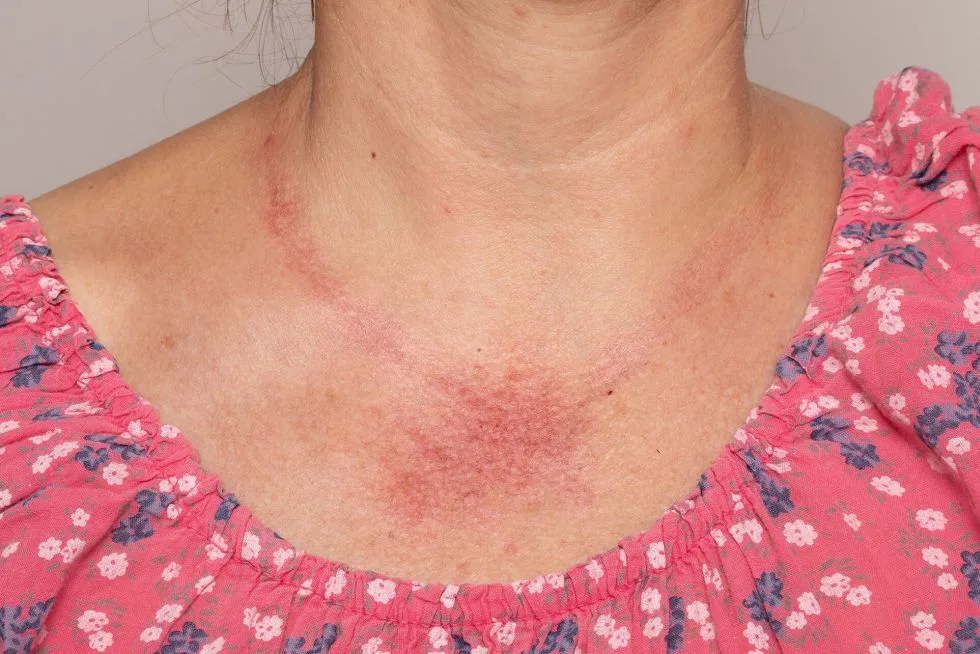
Często z insulinoopornością współistnieją zmiany skórne, na przykład włókniaki, czyli zmiany łagodne. Okazuje się, iż u osób z insulinoopornością i u cukrzyków są częstsze niż w populacji ogólnej. Są to nietypowe objawy, których nikt nie łączy z tym stanem i nie szuka przyczyny, ponieważ są to zmiany łagodne.

6. Czy insulinooporność może być spowodowana niedoczynnością tarczycy? To pytanie od pacjentki, która od dawna choruje na niedoczynność tarczycy, a niedawno okazało się, że ma również insulinooporność.
Niedoczynność tarczycy i IO mogą ze sobą współistnieć. Jedna i druga przypadłość są coraz częstsze w naszej populacji. Duża część moich pacjentów cierpi na jedno i drugie, ale to nie jest tak, że jedno z drugiego wynika. Jaki jest więc między nimi związek? Niewyrównana niedoczynność tarczycy będzie powodowała przyrost masy ciała (przy niedoczynności tarczycy pacjentki mówią, że „tyją od listka sałaty” albo „tylko patrząc na jedzenie”), będzie wpływać na nasz metabolizm, dlatego w którymś momencie może pojawić się insulinooporność. Ale to nie jest tak, że jedna choroba wywołuje drugą.
Winien jest nasz współczesny tryb życia. Coraz mniej się ruszamy, coraz bardziej się najadamy, coraz gorzej jemy, więc tak naprawdę jeśli chodzi o insulinoporność, to sami tworzymy błędne koło.
Jeśli chodzi o przyczyny insulinooporności, to 50% zależy od genetyki i tutaj nie jesteśmy w stanie nic zmienić, mamy takie albo inne geny. Natomiast druga część to jest aktywność fizyczna i nasza dieta, czyli to są te czynniki, które możemy zmienić i które niestety mocno kuleją w obecnych czasach. Pacjentki często mi mówią, że wychodzą z mieszkania i wsiadają do windy, zjeżdżają do garażu podziemnego, jadą samochodem do pracy, tam znów wsiadają do windy. Pracują cały dzień przy biurku, wracają, jak już jest wieczór i trzeba się tylko zająć codziennymi sprawami i idą spać. No i tego ruchu jest bardzo mało. Czasami najprostszą rzeczą, żeby ocenić, ile go mamy, jest po prostu liczenie kroków, większość telefonów ma taką aplikację. Okazuje się, że robimy tylko 1 000 kroków w ciągu dnia, a rekomenduje się 10 000, przy czym tak naprawdę 7 000 kroków dziennie to jest już bardzo przyzwoity wynik. Nie musimy codziennie chodzić na siłownię, ale my obecnie nie mamy nawet tego codziennego ruchu. Wszystko jest blisko, po zakupy jedziemy samochodem, mamy łatwy dostęp do niedrogiego jedzenia, przy wszystkich kasach w supermarketach są słodycze. I nie trzeba nawet mieć złych genów, żeby być jak ta rodzina z jamnikiem. Niestety nasz organizm nie jest przyzwyczajony do takiego trybu życia i po prostu nie daje sobie rady.
Przeczytaj też: Insulinooporność – wstęp do stanu przedcukrzycowego i cukrzycy typu 2